
- Kirjoittaja Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Viimeksi muokattu 2025-01-22 16:58.
Tämä tarkoittaa yleensä sitä, että vesiliuoksessa normaalilämpötilassa ja -paineessa hydronium-ionien pitoisuus on yhtä suuri kuin vahvaa happoa tutustuttiin ratkaisuun. ionisaatio hapot ja pohjat sisään vettä : A vahva happo ionisoituu kokonaan vesiliuoksessa menettämällä yhden protonin (H+).
Vastaavasti, miksi vahvat hapot hajoavat kokonaan vedessä?
Kun HCl-molekyylit liukenevat ne dissosioitua osaksi H+ ionit ja Cl- ioneja. HCl on a vahvaa happoa koska se dissosioituu melkein täysin . Yhteenvetona: mitä vahvempi happoa mitä vapaampi H+ ionit vapautuvat liuokseen. Mitä suurempi on vapaan H:n määrä+, sitä pienempi pH-arvo sille on happoa.
Lisäksi miksi hapot ionisoituvat vedessä? Hapot ja emäkset liukenevat vettä ja koska ne lisäävät yhden tuotteen pitoisuutta vettä itse ionisaatio , joko protoneja tai hydroksidi-ioneja, ne tukahduttavat vettä dissosiaatio. Mille tahansa happoa , Ka on tasapainovakio happoa dissosiaatioreaktio sisään vettä.
Voidaan myös kysyä, ionisoituvatko vahvat hapot kokonaan vedessä?
An happoa tai pohjan vahvuus viittaa sen asteeseen ionisaatio . A vahvaa happoa tahtoa ionisoitua täysin vedessä kun taas heikko happoa tulee vain osittain ionisoida . Vahvempi happoa on parempi protoniluovuttaja, joka pakottaa tasapainon oikealle. Tämä tuottaa enemmän hydroniumioneja ja konjugaattiemästä.
Miksi vahvat hapot ionisoituvat täysin?
A vahvaa happoa on happoa mikä on täysin ionisoitunut vesiliuoksessa. Kloorivety (HCl) ionisoituu täysin vetyioneiksi ja kloridi-ioneiksi vedessä. Heikot hapot , Kuten vahvoja happoja , ionisoida luovuttaa H+ ioni ja konjugaattiemäs. Koska HCl on a vahvaa happoa , sen konjugaattiemäs (Cl−) on erittäin heikko.
Suositeltava:
Miksi koheesio on tärkeää vedessä?

Koheesio mahdollistaa pintajännityksen kehittymisen, jolloin aineen kyky kestää repeytymistä jännityksen tai jännityksen alaisena. Tästä syystä vesi muodostaa pisaroita, kun se asetetaan kuivalle pinnalle sen sijaan, että se litistyisi painovoiman vaikutuksesta
Mitä ovat hapot, emäkset ja suolat?

Happo määritellään aineeksi, jonka vesiliuos maistuu happamalta, muuttaa sinisen lakmuspunaisen ja neutraloi emäksiä. Suola on neutraali aine, jonka vesiliuos ei vaikuta lakmukseen. Faradayn mukaan: happoja, emäksiä ja suoloja kutsutaan elektrolyyteiksi
Mitkä ovat yleisimmät vahvat pohjat?

Tässä on luettelo yleisimmistä vahvoista emäksistä. LiOH - litiumhydroksidi. NaOH - natriumhydroksidi. KOH - kaliumhydroksidi. RbOH - rubidiumhydroksidi. CsOH - cesiumhydroksidi. *Ca(OH)2 - kalsiumhydroksidi. *Sr(OH)2 - strontiumhydroksidi. *Ba(OH)2 - bariumhydroksidi
Miksi suola vedessä on kemiallinen muutos?

Miksi suolan liuottaminen on kemiallinen muutos Siksi suolan liuottaminen veteen on kemiallinen muutos. Kun sokeri liukenee, molekyylit hajaantuvat kaikkialle veteen, mutta ne eivät muuta kemiallista identiteettiään
Miksi vedessä on negatiivinen kaltevuusvaihekaavio?
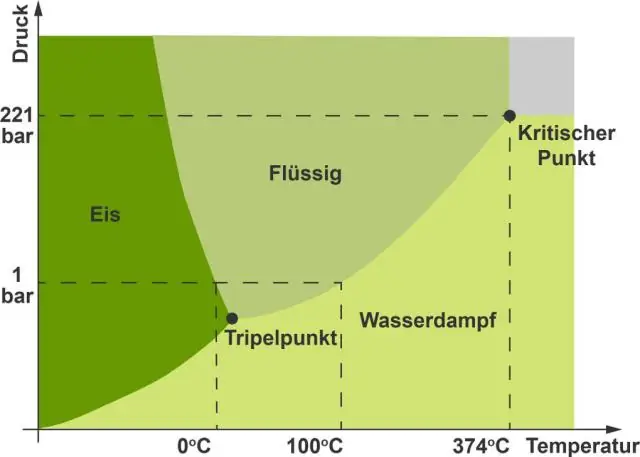
Veden kaaviossa kiinteän ja nestemäisen tilan välisen viivan kaltevuus on negatiivinen pikemminkin kuin positiivinen. Syynä on, että vesi on epätavallinen aine, koska sen kiinteä tila on vähemmän tiheä kuin nestemäinen tila
