- Kirjoittaja Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Viimeksi muokattu 2025-01-22 16:58.
Voit ratkaista tiivistetyn tai laimean liuoksen pitoisuuden tai tilavuuden käyttämällä yhtälö : M1V1 = M2V2 , jossa M1 on väkevöidyn liuoksen pitoisuus molaarisesti (moolia/litraa), V2 on väkevöidyn liuoksen tilavuus, M2 on laimean liuoksen konsentraatio molaarisesti (moolimäärän jälkeen
Vastaavasti saatat kysyä, miksi m1v1 m2v2 toimii?
Vain pitoisuus muuttuu ja tilavuus muuttuu. Liuenneen aineen moolimäärä pysyy vakiona, ellet lisää liuennutta ainetta! Joten suhde perustuu siihen, että liuenneen aineen moolimäärä pysyy vakiona, mutta koko liuoksen pitoisuus ja tilavuus voivat muuttua.
Myöhemmin kysymys kuuluu, kuinka käytät n1v1 n2v2 -kaavaa? N1V1 (HCl) = N2V2 (Na2CO3) tai N1 × 10 = 0,2 × 25 ∴ N1 = 5 / 10 = 0,5 N Normaliteetti × ekvivalenttipaino = lujuus grammoina litrassa. 0,5 × 36,5 = 18,25. HCl-liuoksen vahvuus on 18,25 grammaa litrassa.
Sitä paitsi, mikä on titrauskaava?
Käytä titrauskaava . Jos titrausaineen ja analyytin moolisuhde on 1:1, kaava on hapon molaarisuus (M) x hapon tilavuus (V) = emäksen molaarisuus (M) x emäksen tilavuus (V). (Molaarisuus on liuoksen pitoisuus ilmaistuna liuenneen aineen moolien lukumääränä liuosta litrassa.)
Kuinka käytät m1v1 m2v2:ta?
Voit ratkaista tiivistetyn tai laimean liuoksen pitoisuuden tai tilavuuden käyttämällä yhtälö: M1V1 = M2V2 , jossa M1 on väkevöidyn liuoksen pitoisuus molaarisesti (moolia/litraa), V2 on väkevöidyn liuoksen tilavuus, M2 on laimean liuoksen pitoisuus molaarisesti
Suositeltava:
Mikä on ympyrän pi:n kaava?

Käytä kaavaa. Ympyrän ympärysmitta löytyy kaavasta C= π*d = 2*π*r. Siten pi on yhtä kuin ympyrän ympärysmitta jaettuna sen halkaisijalla
Mikä on yhdisteen nimi, jolla on kaava CuCrO4?
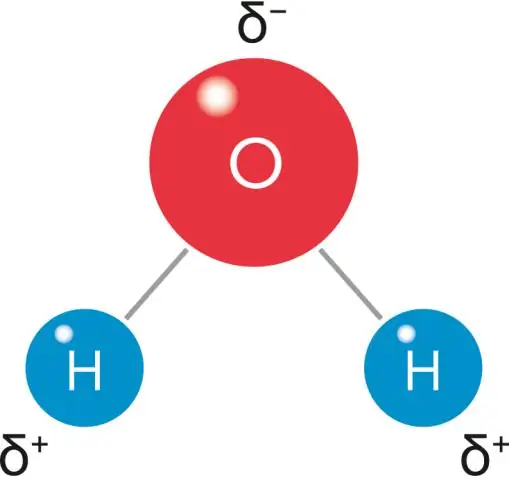
Kupari(II)kromaatti CuCrO4 Molekyylipaino --EndMemo
Mikä on oktaanin empiirinen kaava?

C8H18 Mikä tässä on oktaanin c8h18 empiirinen kaava? The oktaanin empiirinen kaava $$C_{8}H_{18}$$ on: A. B. C. Samoin mikä on c2h6o2:n empiirinen kaava? Molekyyli- ja empiiriset kaavat Kysymys Vastaus Kirjoita empiirinen kaava seuraavalle yhdisteelle:
Mikä on Sin Cos Tan -kaava?
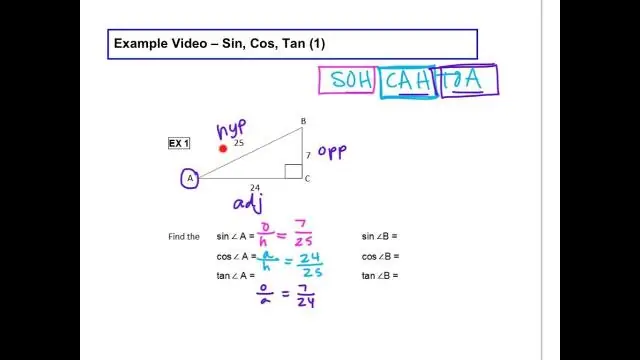
Sinin, cosin ja tan funktiot voidaan laskea seuraavasti: Sinifunktio:sin(θ) = Vastakkainen / Hypotenuusa. Kosinifunktio: cos(θ) = Vierekkäinen / Hypotenuse. Tangenttifunktio: tan(θ) = Vastakkainen / Vierekkäinen
Mikä on kofeiinin empiirinen kaava?
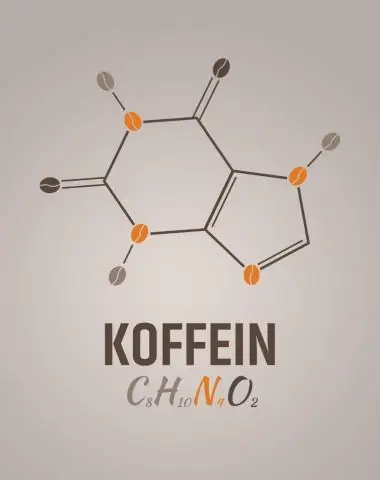
2 vastausta. C8H10N4O2 on kofeiinin molekyylikaava
