
- Kirjoittaja Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Viimeksi muokattu 2025-01-22 16:58.
Proteiinin tertiäärinen rakenne viittaa sen polypeptidiketjun yleiseen kolmiulotteiseen järjestykseen avaruudessa. Se on yleensä stabiloitu ulkopuolisella polaarisella hydrofiilisellä vety ja ionisidosvuorovaikutukset ja sisäiset hydrofobiset vuorovaikutukset ei-polaaristen aminohapposivuketjujen välillä (kuvio 4-7).
On myös tiedettävä, kuinka ionisidokset stabiloivat tertiäärisiä rakenteita?
Ylläpitävät vuorovaikutukset Kolmannen asteen rakenne Suolasillat: Proteiini taittuu niin, että positiivisesti varautuneita sivuketjuja ovat sijaitsevat usein vierekkäin to negatiivisesti varautuneita sivuketjuja. Suolasilta tai ionisidos varattujen funktionaalisten ryhmien välillä auttaa vakauttaa the tertiäärinen rakenne.
Lisäksi mitkä kemialliset sidokset stabiloivat primaaristen sekundaaristen tertiääristen ja kvaternaaristen rakenteiden eri rakenteita? Kuten disulfidisillat, nämä vety joukkovelkakirjat voi yhdistää kaksi ketjun osaa, jotka ovat järjestyksessä jonkin matkan päässä. Suolasillat, ionivuorovaikutukset positiivisesti ja negatiivisesti varautuneiden kohtien välillä aminohapposivuketjuissa, auttavat myös vakauttaa the tertiäärinen rakenne proteiinista.
Mitkä proteiinirakenteen tasot tällä tavalla stabiloituvat vetysidoksilla?
Kolmannen asteen rakenne On olemassa useita erilaisia sidoksia ja voimia, jotka pitävät proteiinia sisällään tertiäärinen rakenne . Vetysidos polypeptidiketjussa ja aminohappo "R"-ryhmien välillä auttaa stabiloimaan proteiinin rakennetta pitämällä proteiinin hydrofobisten vuorovaikutusten muodostamassa muodossa.
Mitkä joukkovelkakirjat ovat tertiaarisessa rakenteessa?
Proteiinin tertiäärinen rakenne koostuu tavasta, jolla polypeptidi muodostuu monimutkaisesta molekyylimuodosta. Tämä johtuu R-ryhmän vuorovaikutuksista, kuten ionisista ja vetysidoksia , disulfidisillat ja hydrofobiset ja hydrofiiliset vuorovaikutukset.
Suositeltava:
Kuka keksi DNA-kyselyn rakenteen?
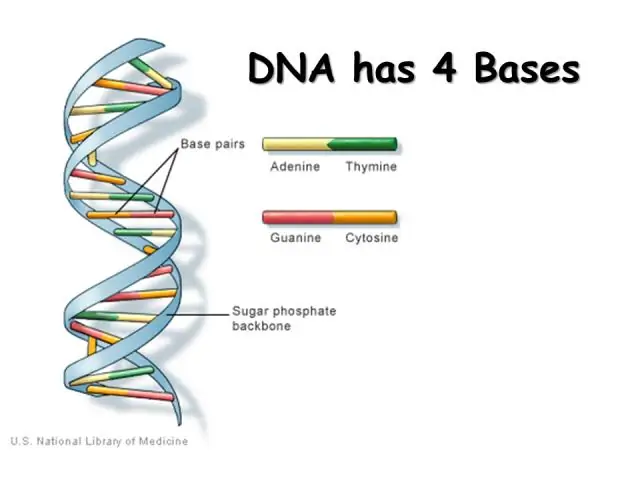
Tiedemiehet pitivät DNA:n rakenteen löytämisen ansiota (julkaistu 1953 Naturessa). Vaikka Watsonin ja Crickin ansioksi annettiin löytö, he eivät olisi tienneet rakenteesta, elleivät he olisi nähneet Rosalind Franklinin ja Maurice Wilkinsin tutkimusta
Mikä on rakenteen ja toiminnan välinen suhde?

Biologiassa keskeinen ajatus on, että rakenne määrää toiminnan. Toisin sanoen tapa, jolla jokin on järjestetty, mahdollistaa sen, että se voi täyttää tehtävänsä eliössä (elämässä). Rakenteen ja toiminnan väliset suhteet syntyvät luonnollisen valinnan prosessin kautta
Mikä on kloorin sitoutuminen?

Kloori on ei-metalli. Klooriatomin ulkokuoressa on 7 elektronia. muiden klooriatomien kanssa. Yksi jaettu elektronipari muodostaa yhden kovalenttisen sidoksen
Mikä voima vaikuttaa eniten proteiinin tertiaarisen rakenteen määrittämiseen?

Proteiinin tertiäärinen rakenne on proteiinin kolmiulotteinen muoto. Disulfidisidokset, vetysidokset, ionisidokset ja hydrofobiset vuorovaikutukset vaikuttavat kaikki proteiinin muotoon
Mikä aminohappo stabiloi proteiinin tertiaarista rakennetta?

Nämä vuorovaikutukset ovat mahdollisia laskostumalla proteiiniketjuun tuomaan kaukaiset aminohapot lähemmäksi toisiaan. 2. Tertiääristä rakennetta stabiloivat disulfidisidokset, ionivuorovaikutukset, vetysidokset, metallisidokset ja hydrofobiset vuorovaikutukset
