
- Kirjoittaja Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Viimeksi muokattu 2025-01-22 16:58.
Rikkiheksafluoridilla on keskus rikki atomi minkä ympärillä voi katso 12 elektronia tai 6 elektroniparia. Näin ollen SF6-elektronigeometria On katsotaan olevan oktaedri . Kaikki F-S-F-sidokset ovat 90 astetta ja se on ei yksinäisiä pareja.
Kun tämä otetaan huomioon, miksi sf6:lla on oktaedrinen muoto?
An oktaedri Molekyyli koostuu keskusatomista, joka on sitoutunut kuuteen atomiin, ilman yksittäisiä elektronipareja. Valence Shell Electron Pair Repulsion Theory (VSEPR) -teorian mukaan elektroniparit hylkivät toisiaan riippumatta siitä, ovatko ne sidoksissa vai yksittäisinä pareina. Kaikki sidoskulmat muodostuvat oktaedri molekyyli on 90 astetta.
Myöhemmin kysymys kuuluu, mitä on hybridisaatio ja sf6-molekyylin muodon piirtäminen? SF6 näyttää sp3d2 hybridisaatio . The rakenne on oktaedrinen. Jokainen sp3d2-orbitaali limittyy 2-fluoriporbitaalin kanssa muodostaen SF-sidoksen.
Samalla tavalla voidaan kysyä, minkä geometrian ennustaisit rikkiheksakloridille?
Molekyyli geometria / rikkiheksafluoridi on oktaedrinen. Keskusatomi rikki muodostivat yksinkertaisen sidoksen kuudella fluoriatomilla. Se on vapautettu oktettisäännöstä, koska rikki on iso atomi.
Mikä on XeF4:n Lewis-rakenne?
Kaksi sitoutumatonta elektroniparia on asetettu kohtisuoralle akselille. Kaikki nämä muodostelmat kutsutaan neliön taso XeF4 Lewis -rakenne siinä on yhteensä 36 valenssielektronia.
Suositeltava:
Mikä on yksinkertaisin muoto 6 20:lle?

Yksinkertaista 6/20 yksinkertaisimpaan muotoon. Online yksinkertaistettu murtolukulaskin vähentää 6/20 alhaisimpiin termeihin nopeasti ja helposti. 6/20 Yksinkertaistettu vastaus: 6/20 = 3/10
Miksi kiinteällä aineella on kiinteä muoto ja tilavuus?

1 vastaus. Kiinteillä aineilla on kiinteä muoto ja niillä on kiinteä tilavuus. Koska nesteiden hiukkaset ovat hyvin lähellä toisiaan (tuskin kauempana kuin kiinteissä aineissa), nesteet eivät puristu helposti kokoon, joten niiden tilavuus on kiinteä. Kaasut voivat myös virrata, joten ne täyttävät koko säiliönsä muodon
Kuinka muunnetaan yleinen muoto hyperbolin vakiomuodoksi?

Sivulle avautuvan hyperbolin standardimuoto on (x - h)^2 / a^2 - (y - k)^2 / b^2 = 1. Ylös- ja alaspäin avautuvalle hyperbolille se on (y - k) ^2 / a^2 - (x- h)^2 / b^2 = 1. Molemmissa tapauksissa hyperbolaan (h, k) antama keskipiste
Mikä on yksinkertaisin muoto luvulle 7 10?

710 on jo yksinkertaisimmassa muodossa. Se voidaan kirjoittaa 0,7 desimaalimuodossa (pyöristetty 6 desimaaliin)
Miten kasvisolun muoto eroaa eläinsolun muodosta?
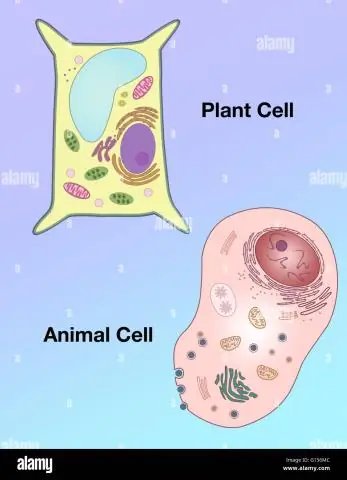
Vakuolit: Kasvisoluilla on suuri tyhjiö, kun taas eläinsoluissa on useita pieniä tyhjiöitä. Muoto: Kasvisoluilla on säännöllisempi muoto (yleensä suorakaiteen muotoinen), kun taas eläinsoluilla on epäsäännöllinen muoto. Lysosomit: ovat yleensä läsnä eläinsoluissa, kun taas ne puuttuvat kasvisoluista
