- Kirjoittaja Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Viimeksi muokattu 2025-01-22 16:58.
A molekyylikaava käyttää kemiallisia symboleja ja alaindeksejä osoittamaan tarkat numerot eri atomeja molekyylissä tai yhdiste. Empiirinen kaava antaa atomien yksinkertaisimman kokonaislukusuhteen jonkin sisällä yhdiste. A rakennekaava ilmaisee atomien sitoutumisjärjestelyn molekyylissä.
Tiedä myös, mitä eroa on molekyyli- ja rakennekaavojen välillä?
The molekyylikaavat näytä kunkin atomityypin oikea numero molekyylissä . Elektronipistekaaviot (Lewis rakenteet ) osoittavat näiden atomien ja kaikkien valenssielektronien sijoittelun. The rakennekaavat osoittavat atomien ja kovalenttisten sidosten järjestyksen välillä niitä.
Mikä on rakennekaavaesimerkki yllä olevan lisäksi? Kemikaali kaava joka osoittaa, kuinka yhdisteen muodostavat atomit ovat järjestetty molekyyliin. varten esimerkki , rakennekaava aspiriinista on CH3COOC6H4COOH, mikä osoittaa, että se koostuu asetyyliryhmästä (CH3COO), joka on kiinnittynyt fenyyliryhmän karboksyylihappoon (COOH) (C6H4). Vertaa empiiristä kaava.
Lisäksi mitkä molekyylin ominaisuudet täydellinen rakennekaava ilmaisee, mitä molekyylikaava ei?
Molekyylikaavat sisältää ei tietoa atomien järjestyksestä. A rakennekaava On ei yhtä kompakti ja helppokäyttöinen kommunikoida , mutta se tarjoaa tietoa siitä, että molekyylikaava ei atomien suhteellisesta sijainnista ja atomien välisestä sidoksesta.
Mitä eroa on rakenteellisen ja näytetyn kaavan välillä?
A rakennekaava näyttää kuinka eri atomit ovat sitoutuneet. On olemassa useita tapoja piirtää tämä, ja sinun on tunnettava ne kaikki. A näytettävä kaava näyttää kaikki joukkovelkakirjat in molekyyli yksittäisinä juovina. Sinun on muistettava, että jokainen viiva edustaa jaettua elektroniparia.
Suositeltava:
Mitä eroa on korrelaation ja chi-neliön välillä?
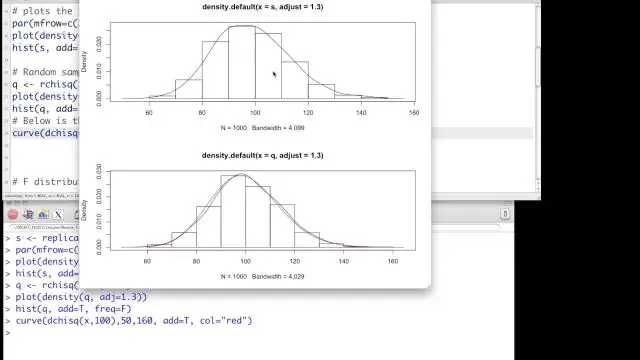
Joten korrelaatiossa on kyse kahden muuttujan välisestä lineaarisesta suhteesta. Yleensä molemmat ovat jatkuvia (tai melkein niin), mutta tapauksiin, joissa toinen on kaksijakoinen, on vaihteluita. Chi-neliö tarkoittaa yleensä kahden muuttujan riippumattomuutta. Yleensä molemmat ovat kategorisia
Mitä eroa on ilmastovyöhykkeen ja biomin välillä?

Ilmasto luokitellaan ilmakehän lämpötilan ja sateen perusteella, kun taas biomi luokitellaan ensisijaisesti yhtenäisten kasvillisuustyyppien perusteella. Ilmasto voi määrittää, mitä biomi on läsnä, mutta biomi ei yleensä hallitse tai vaikuta ilmastoon samalla tavalla
Mikä on täydellinen rakennekaava?

Täydelliset rakennekaavat. Täydelliset rakennekaavat näyttävät kaikki molekyylin atomit, ne yhdistävät sidostyypit ja kuinka ne ovat yhteydessä toisiinsa. Yksinkertaiselle molekyylille, kuten vesi, H2O, molekyylikaava, tulee H-O-H, rakennekaava
Kuinka kirjoitat tiivistetyn rakennekaavan?
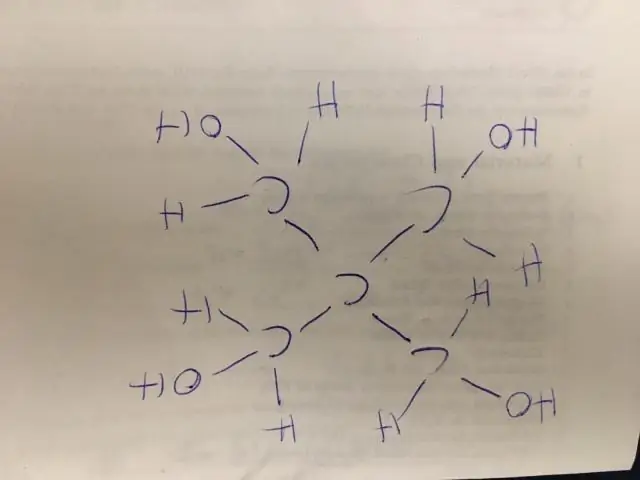
1 Vastaus Kirjoita pisimmän ketjun atomit vaakasuoraan siinä järjestyksessä, jossa ne liittyvät toisiinsa. Kirjoita kaikki ligandit atomille välittömästi sen oikealle puolelle, ja kerro niiden alaindeksit. Merkitse polyatomiset ligandit sulkeisiin. Käytä erityisiä sidoksia tarvittaessa selventämään liitteitä
Mitä eroa on hetkellisen ja keskinopeuden välillä, mikä on suurin esimerkki hetkellisestä nopeudesta?

Keskinopeus on nopeus, joka on laskettu keskiarvona ajanjaksolle. Hetkellinen nopeus olisi nopeus missä tahansa hetkessä kyseisellä aikavälillä mitattuna reaaliaikaisella nopeusmittarilla
