
- Kirjoittaja Miles Stephen stephen@answers-science.com.
- Public 2024-01-18 08:15.
- Viimeksi muokattu 2025-01-22 16:58.
- Piirrä ydin.
- Kirjoita ytimessä olevien neutronien ja protonien lukumäärä.
- Piirrä ensimmäinen energiataso.
- Piirrä energiatasojen elektronit alla olevien sääntöjen mukaisesti.
- Pidä kirjaa siitä, kuinka monta elektronia on sijoitettu kullekin tasolle ja kuinka monta elektronia on jäljellä käytössä.
Kun tämä otetaan huomioon, kuinka Bohrin kaaviot toimivat?
Bohrin kaavioita osoittavat elektroneja, jotka kiertävät atomin ydintä hieman samalla tavalla kuin planeetat kiertävät aurinkoa. Vuonna Bohrin malli , elektronien kuvataan liikkuvan ympyröissä eri kuorilla riippuen siitä, mikä elementti sinulla on. Jokainen kuori voi sisältää vain tietyn määrän elektroneja.
Samoin kuinka monta elektronia on kuoressa? Jokainen kuori voi sisältää vain kiinteän määrän elektroneja: Ensimmäinen kuori voi sisältää enintään kaksi elektronia , toinen kuori mahtuu kahdeksan (2 + 6) elektronia, kolmas kuori mahtuu enintään 18 (2 + 6 + 10) ja niin edelleen. Yleinen kaava on, että n:s kuori voi periaatteessa pitää sisällään jopa 2(n2) elektroneja.
Vastaavasti mikä on Bohrin diagrammi?
Bohr-kaavio on yksinkertaistettu visuaalinen esitys atomista, jonka tanskalainen fyysikko Niels Bohr kehitti vuonna 1913. Kaavio kuvaa atomin positiivisesti varautuneena ydin ympäröimä elektroneja jotka kulkevat ympyräradalla ympäri ydin erillisillä energiatasoilla.
Kuinka luet Bohrin mallia?
- Piirrä ydin.
- Kirjoita ytimessä olevien neutronien ja protonien lukumäärä.
- Piirrä ensimmäinen energiataso.
- Piirrä energiatasojen elektronit alla olevien sääntöjen mukaisesti.
- Pidä kirjaa siitä, kuinka monta elektronia on sijoitettu kullekin tasolle ja kuinka monta elektronia on jäljellä käytössä.
Suositeltava:
Miksi Bohr muutti Rutherfordin atomimallia?

Bohrin atomimalli: Vuonna 1913 Bohr ehdotti atomin kvantisoitua kuorimalliaan selittääkseen, kuinka elektroneilla voi olla vakaat kiertoradat ytimen ympärillä. Vakausongelman korjaamiseksi Bohr muokkasi Rutherfordin mallia vaatimalla, että elektronit liikkuvat kiinteän koon ja energian kiertoradoilla
Kuinka Bohr muuttaa Rutherfordin mallia?

Vakausongelman korjaamiseksi Bohr muokkasi Rutherfordin mallia vaatimalla, että elektronit liikkuvat kiinteän koon ja energian kiertoradoilla. Elektronin energia riippuu kiertoradan koosta ja on pienempi pienemmillä kiertoradoilla. Säteilyä voi tapahtua vain, kun elektroni hyppää kiertoradalta toiselle
Kuinka piirrät nopeus vs aika -kaavion?
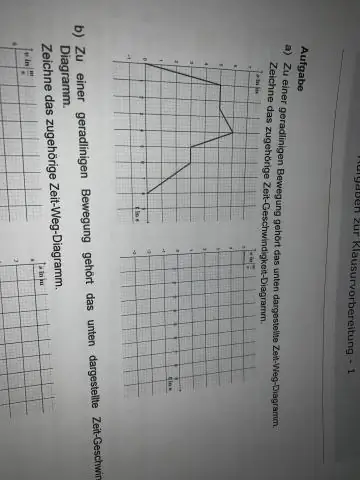
Piirrä millimetripaperille kaksi suoraa, jotka alkavat samasta pisteestä ja ovat kohtisuorassa toisiinsa nähden. Tämä on x-y-akseli. X-akseli on vaakaviiva ja y-akseli on pystysuora viiva. Merkitse sopivat tasaväliset aikavälit x-akselille, jotta voit helposti piirtää aika-arvot taulukosta
Miten Bohr paransi Rutherfordin atomimallia?

Bohr paransi Rutherfordin atomimallia ehdottamalla, että elektronit kulkivat ympyräradalla tietyillä energiatasoilla. Selitys: Rutherford ehdotti, että elektronit kiertävät ydintä kuten planeetat auringon ympäri. Kun metalliatomia kuumennetaan, se absorboi energiaa ja elektronit hyppäävät korkeammalle energiatasolle
Kuinka piirrät etäisyys vs aika -kaavion?
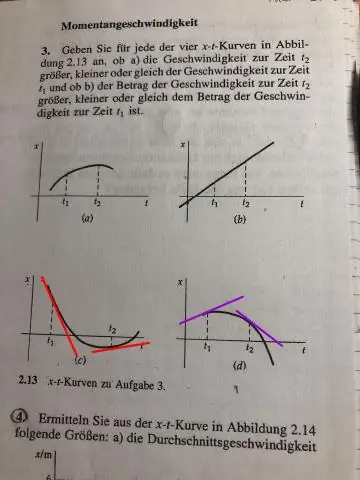
Etäisyys Aika -kaavio on viivakaavio, joka ilmaisee etäisyyden vs. aika -havainnot kuvaajasta. Etäisyys-aikakaavion piirtäminen on yksinkertaista. Tätä varten otamme ensin graafisen paperin arkin ja piirretään siihen kaksi kohtisuoraa viivaa, jotka liittyvät O:een. Vaakaviiva on X-akseli, kun taas pystysuora on Y-akseli
