
- Kirjoittaja Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:36.
- Viimeksi muokattu 2025-06-01 05:04.
Arrhenius Yhtälö : ln k = -Ea/R (1/T)+ ln (A)<----- tämä on y = mx + b -muoto yhtälö , mutta minulla on vaikeuksia ymmärtää, miten se ratkaistaan. ln k = -0,0008313/8,314 J/mol K (1/298 K ) + ln (-0.8794) <---- näin asetin numerot, mutta en pidä sitä oikein
Tästä, mikä on Ln K kemiassa?
lnk = ln (Ae−Ea/RT)= ln A+ ln (e−Ea/RT) lnk = ln A+−EaRT=(−EaR)(1T)+ ln A. joka on yhtälö suorasta viivasta, jonka kaltevuus on -Ea /R. Tämä tarjoaa yksinkertaisen tavan määrittää aktivointienergia arvoista k havaitaan eri lämpötiloissa piirtämällä lnk funktiona 1/T.
Lisäksi mikä on nopeusvakio k? The nopeusvakio , k , on suhteellisuusperiaate vakio joka osoittaa suhteen reagoivien aineiden moolipitoisuuden ja korko kemiallisesta reaktiosta.
Ihmiset myös kysyvät, mikä on aktivointienergian kaava?
Aktivointienergian määrittäminen. Huomaa, että kun Arrhenius-yhtälö järjestetään uudelleen kuten yllä, se on lineaarinen yhtälö, jonka muoto on y = mx + b; y on ln(k), x on 1/T ja m on -Ea/R. Reaktion aktivointienergia voidaan määrittää etsimällä kaltevuus linjasta.
Mitkä ovat nopeusvakion k yksiköt?
The yksiköitä / k riippuu reaktion järjestyksestä, mutta yksiköitä eivät koskaan ole Newtoneja metriä kohti. Esimerkkinä ensimmäisen asteen reaktiosta k on yksiköitä 1/s ja toisen asteen reaktiolle, yksiköitä 1/M.s.
Suositeltava:
Kuinka lasket keskihajonnan PMP:stä?

PMBOK:ssa käytetty standardipoikkeama kaava on yksinkertainen. Se on vain (P-O)/6. Tämä on pessimistinen aktiivisuusarvio miinus optimistinen aktiivisuusarvio jaettuna kuudella. Ongelmana on, että tämä muoto tai muoto ei millään tavalla tuota keskihajonnan mittaa
Kuinka lasket Maan ympärysmitan leveysasteella?

Ympyrän ympärysmitta on 2πr, missä r on sen säde. Maapallolla pallon ympärysmitta tietyllä leveysasteella on 2πr(cos θ), missä θ on leveysaste ja r on maan säde päiväntasaajalla
Kuinka lasket taajuuden taajuudesta ja prosenteista?
Tätä varten jaetaan taajuus tulosten kokonaismäärällä ja kerrotaan 100:lla. Tässä tapauksessa ensimmäisen rivin taajuus on 1 ja tulosten kokonaismäärä on 10. Prosenttiosuus olisi tällöin 10,0. Viimeinen sarake on kumulatiivinen prosenttiosuus
Kuinka lasket potentiaalin pudotuksen piirissä?
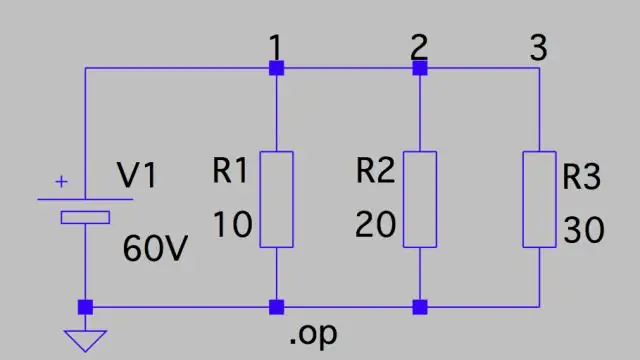
Jännitehäviö: Rinnakkaispiiri Tämä tarkoittaa, että jännitehäviö kunkin kohdalla on vain piirin kokonaisjännite jaettuna piirissä olevien vastusten lukumäärällä tai 24 V/3 = 8 V
Kuinka lasket kattoontelon suhteen?

Vaiheet: Huoneen onkalosuhde = 2,9; kattoontelosuhde = 0,0 (upotetut lamput); lattian ontelosuhde = 1,2 (eli 20 x 30 x 3' syvyydelle) Tehokas kattoheijastus =. 80; Tehokas lattiaheijastus =
