
- Kirjoittaja Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Viimeksi muokattu 2025-01-22 16:58.
Miten vesi eroaa sulamispisteensä alapuolella ja sen yläpuolella se? Alla se pysyy lähellä toisiaan ja ne pomppivat pois toisistaan. Edellä molekyylit pääsevät vielä lähemmäksi kuin alla . The kiehuvaa /tiivistyminen kohta / vettä on 373K.
Miksi sulamis- ja jäätymispisteet ovat samat?
Jäätymistä ja sulaminen ovat vain erilaisia termejä, joita käytetään kuvaamaan siirtymää materiaalin kiinteän ja nestemäisen tilan välillä. Jäätymistä tarkoittaa yleensä sitä, että materiaalista poistetaan energiaa (neste muuttuu kiinteäksi) ja sulaminen tarkoittaa yleensä sitä, että materiaaliin lisätään energiaa (kiinteä aine muuttuu nesteeksi).
Voidaan myös kysyä, alentaako vesi sulamispistettä? Sulaminen imee lämpöä ("piilevä lämpö"), koska nesteessä on enemmän energiaa kuin kiinteässä aineessa. Se jäähdyttää jäätä ja suolaista vettä alle 0°C. Joten kyllä, se alentaa todellinen lämpötila.
Vastaavasti voit kysyä, mistä tiedät, onko yhdisteen sulamispiste huoneenlämpötilan ylä- vai alapuolella?
Jos the aineen normaali sulamispiste On huoneenlämpötilan alapuolella , aine on nesteenä huonelämpötila . Bentseeni sulaa 6 °C:ssa ja kiehuu 80 °C:ssa; se on nestettä huonelämpötila . Jos molemmat normaali sulamispiste ja normaali kiehumispiste ovat huoneenlämpötilan yläpuolella , aine on kiinteä.
Millä aineella on korkeampi sulamispiste kuin vedellä?
Natriumkloridi sulaa 801 °C:ssa. Jää (kiinteä H 2 O) on molekyyliyhdiste, jonka molekyylejä pitää yhdessä vety joukkovelkakirjat. Vaikka vety sidokset ovat vahvimmat molekyylien väliset voimat, vahvuus vety sidosten määrä on paljon pienempi kuin ionisidosten.
Sulamispiste.
| Materiaali | Sulamispiste (°C) |
|---|---|
| rauta- | 1538 |
Suositeltava:
Miksi puurajan yläpuolella ei ole puita?

Puut eivät kasva puurajan yläpuolella kovien tuulien, alhaisen kosteuden ja kylmien lämpötilojen vuoksi. Puut kasvavat kaikkialla maailmassa, monessa eri säässä. Mutta tiettyjen korkeuksien yläpuolella puut eivät vain voi kasvaa. Pienet puut tarvitsevat vähemmän kosteutta ja vähemmän happea
Miten holeiiittibasaltti eroaa useimmista vulkaanisista kivistä?

Tholeiiittisen magmasarjan kivet luokitellaan subalkalisiksi (ne sisältävät vähemmän natriumia kuin jotkin muut basaltit) ja ne eroavat kalkki-emäksisen magmasarjan kivistä sen magman redox-tilan perusteella, josta ne kiteytyivät (toleiiittiset magmat pelkistyvät; alkaliset magmat hapettuvat)
Miten kovalenttinen sidos eroaa ionisidoskyselystä?

Ero ionisen ja kovalenttisen sidoksen välillä on se, että kovalenttinen sidos muodostuu, kun kaksi atomia jakavat elektroneja. Ionisidokset ovat voimia, jotka pitävät yhdessä sähköstaattiset vetovoimat vastakkaisesti varautuneiden ionien välillä. Ionisidosten elektronegatiivisuuden ero on suurempi tai yhtä suuri kuin 2
Miten kasvisolun muoto eroaa eläinsolun muodosta?
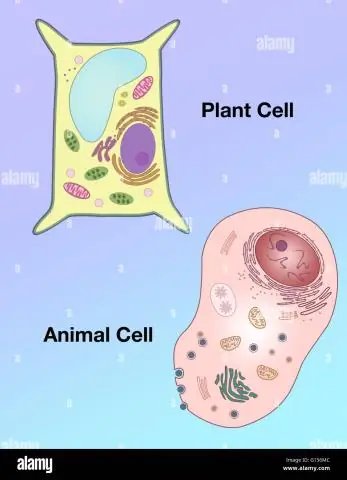
Vakuolit: Kasvisoluilla on suuri tyhjiö, kun taas eläinsoluissa on useita pieniä tyhjiöitä. Muoto: Kasvisoluilla on säännöllisempi muoto (yleensä suorakaiteen muotoinen), kun taas eläinsoluilla on epäsäännöllinen muoto. Lysosomit: ovat yleensä läsnä eläinsoluissa, kun taas ne puuttuvat kasvisoluista
Miten orgaaniset yhdisteet saivat nimensä Miten sana liittyy sen merkitykseen?
Miten sana liittyy sen merkitykseen? Orgaaniset yhdisteet on saanut nimensä hiilisidosten lukumäärästä. Sana liittyy merkitykseen, koska se liittyy orgaanisten yhdisteiden hiiliatomien sidoksiin
